Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124
Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

سنة ١٩٨٨ تقاسم ٣ أشخاص جائزة نوبل للطب . الثلاثة دول هم كان أولهم سير جيمس بلاك من شركة ICI اللي هتبقى بعد كدا جزء من Astrazeneca عن اكتشافه للPropranolol كأول β-blocker . تقاسم الجايزة معاه اتنين علماء من شركة Wellcome اللي هتكون بعد كدا جزء من Glaxo . الاتنين دول هم جيرترود اليون و جورج هتشينجز Gertrude Elion & George Hitchings . الثنائي الامريكي وعلى مدار ٣٠ سنة اشتغلوها مع بعض عملوا عظمة. أهم إنجازاتهم كان انهم طوروا عدد من الادوية من ضمنها ازاثيوبرين Azathioprine . المميز في شغل اليون و هتشينجز انهم اشتغلوا على فكرة واحدة أساسية و توسعوا في تطبيقها . الفكرة دي هي انتاج Antimetabolites .

الفكرة هي اننا هنطور مواد فعالة تشتغل على تعطيل خطوات بناء ال DNA . بمعنى اننا هنستخدم مواد شبه اللي الجسم بيبني بيها الDNA . ولكن هنعدلها بحيث تكون غير صالحة للاستخدام ( تقدر تقول هنوفر للجسم طوب و اسمنت مغشوشين ) . ودا هيتسبب في تعطيل عملية البناء كلها. وفي النهاية هندور هو الطوب البايظ دا آثر على أي خطوة بالضبط في عملية البناء (Mechanism) . ودا هيساعدنا في فهم الخطوات الأضعف و على الأساس دا نحاول نحسن التركيبة وتقليل الأثار الجانبية.
الفكرة في بداية تطبيقها كانت ثورية جدا ، ليه ؟ لأن قبل كدا كان تطوير الأدوية معتمد على مواد طبيعية . وكنا بنعرف بالمصادفة ان ليهم تأثير معين فبدأنا نعدلها و نحسنها عشان نعمل منها دوا . الطريقة القديمة دي هي اللي طلعتلنا الAspirin و NSAIDs و الOpioids و Penicillin antibiotics وغيرها كتير أوي. حتى لو تفتكروا واحنا بنتكلم عن Methotrexate قلنا ان المصدر اللي بدأنا بيه كان Folic acid اللي جاي من الخميرة . و بالتالي فأصل معرفتنا عن مفعول الAntifolates زي Methotrexate نفسه جه بالصدفة .
انما تفكير Elion و Hitchings كان في طريقة ثانية . احنا نشوف المكونات اللي الخلية محتاجاها عشان يبني الDNA و ندخل المعمل نعمل مواد شبيهة . المواد الجديدة هنجربها على خلايا حية من بكتريا عشان نشوفها هل الخلية هتمتصها و هتستخدمها ولا لأ . بعدها نتأكد هل النمو هيقف بعد ما اخدتها وبأي درجة . في الخطوة التالية هناخد المواد اللي نفعت ووقفت النمو و نجربها على حيوانات اكبر لحد ما نوصل لتجربتها على انسان مريض. المهم ان الطوب المضروب هنحاول نحسنه عشان يستهدف بس الخلية المريضة أو يكون استهلاكه أكبر فيها عشان نقلل الآثار الجانبية .
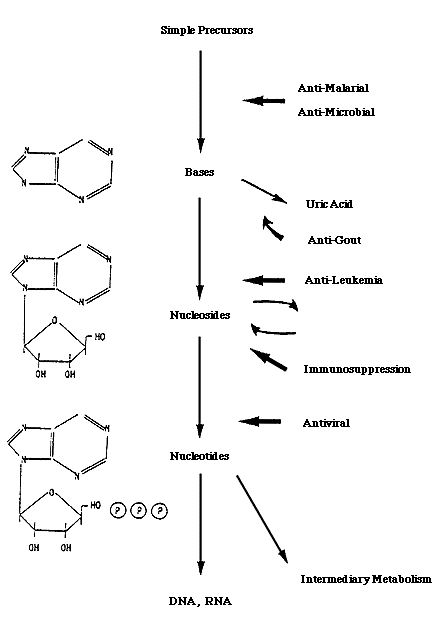
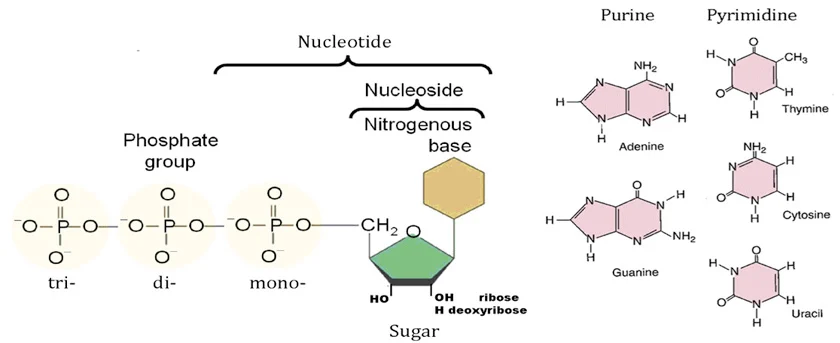
هنا طبعا لازم نسأل طب و ايه المكونات اللي الجسم بيحتاجها عشان يبني DNA . طب خليني اكلمك شوية عن الDNA نفسه و تركيبه . الDNA أو Deoxyribonucleic acid هو عبارة عن شريطين طوال من حمض متكون من سكر الdeoxy Ribose . الشريطين الطوال دول رابط بينهم مجموعات قاعدية Bases فيها نيتروجين في حلقات Heterocyclic.
الBases دي ليها نوعين:
الDNA فيها نوعين اتنين من الPurine bases وهم Adenine و Guanine و نوعين اتنين Pyrimidine bases هم thymine (في RNA بداله Uracil ) و cytosine . ترتيب الاربعة دول على الشريطين هو اللي بيعمل الChromosome و هي دي طريقة الخلية في كتابة شفرتها.
الBases دي لوحدها كدا لو مسكت في جزيء سكر deoxyribose تعمل لنا شكل نسميه Nucleoside.
وعشان الشريطين دول يكتملوا بيحتاجوا مجموعة Phosphate تمسك في جزئ السكر الdeoxyribose من الناحية التانية و بكده بقى عندنا Nucleotide . و الNucleotide هي وحدة بناء ال DNA أو ال RNA .
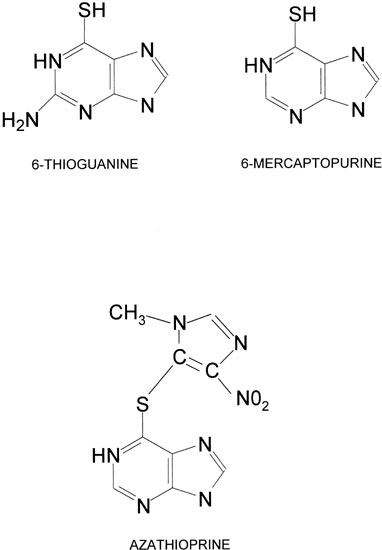
نرجع بقا لElion و Hitchings في أول نجاحاتهم هنلاقيهم هيعملوا في المعمل Base شبه الاتنين Purines . النقطة انهم هيغيروا شوية و يضيفوا Sulfur في الحلقة عشان يطلعولنا مركب اسمه 6MP او mercaptopurine و اللي نعرفه النهارده باسم Purinethol . المركب الجديد اللي نجح في تعطيل نمو الخلايا هيكون من أوائل المواد المستخدمة في العلاج الكيماوي للسرطان في من بداية الخمسينات.
>المركب الجديد 6MP وبرغم نجاحه الكبير هيكون من عيوبه آثاره الجانبية و منها انه بيأثر على المعدة و انه قصير المفعول .
وهنا هيطورلنا الثنائي مركب جديد عبارة عن Mercaptopurine مرتبط بجزئ تاني من حلقة Heterocyclic مش فعالة برابطة ضعيفة . الرابطة الضعيفة دي هتفك لوحدها بدون الحاجة لانزيمات في الامعاء من غير ما الدوا يسبب هناك اثار جانبية و كمان الدوا مفعولة هيطول و هيكون أخف بشكل عام في الآثار الجانبية . المركب الجديد هيكون اسمه Azathioprine و هينزل السوق لنفس التأثير باسم Immuran .
الأثر الجانبي القوى على خلايا المناعة هيلاحظه اكتر من عالم و طبيب منهم Sir Peter Medawar و Sir Roy Calne اللي يعتبروا من اوائل الاطباء اللي عملوا زراعة أعضاء . الدكاترة كانوا ملاحظين ان الجسم بيرفض العضو المزروع و بيبدأ يبني ضده اجسام مضادة و عدد خلايا المناعة بيبدأ يزيد بسرعة . Sir Calne هيجرب Mercaptopurine بس الاعراض الجانبية و قصر المفعول هيعملوله مشكله و هنا هتقترح عليه انه يستخدم بداله المنتج الجديد Azathioprine و اللي كانت نتايجه افضل و اقوى و تم اعتماده في بروتوكولات زراعة الأعضاء بشكل واسه (ولا يزال)
وبالوقت بدأ استخدام Azathioprine ينتشر في الحالات المناعية زي في التهابات القولون خاصة Crohn’s Disease أو حتى في مرض الذئبة الحمراء Systemic Lupus وغيرها .
لكن Azathioprine مكانش أخر انجاز لفريق Wellcome . بعد النجاح فيه لاحظوا ان حتى مع Mercaptopurine فالجسم بيقدر يتخلص من المادة الفعالة بسبب ان الPurines ليها طريقين للMetabolism :
Synthesis : وهنا الجسم بيبني الPurines من مكونات بسيطة في عملية طويلة و دي وجود ال6MP بيوقفها في اكتر من خطوة
Catabolism : وهنا النقطة ان بعد ما اي بعد ما الخليا بتموت الجسم بيحول الPurines لUric acid عشان يخرج في البول ، و بالرغم من انه Mercaptopurine مش Purine طبيعي الا ان الجسم بيقدر يكسره زي ما بيكسر اي Purine تاني و يحوله ل Uric Acid . التكسير دا بيتم عن طريق انزيمات اهمها ال Xanthine oxidase .
وهنا تركيز الثنائي بنفس الأسلوب هيروح للانزيم دا و هيتم فحص هو شغال على مركب وسيط شكله عامل ازاي و هيتم عمل مركب شبيه بهدف تعطيل ال Xanthine Oxidase عشان الMercatopurine يفضل شغال و ما يتكسرش .
و النتيجة : دوا Allopurinol اللي استعماله اتحول من مساعد لMercaptopurine لمنطقة تانية و هي لحالات زيادة اليوريك اسيد و النقرس.
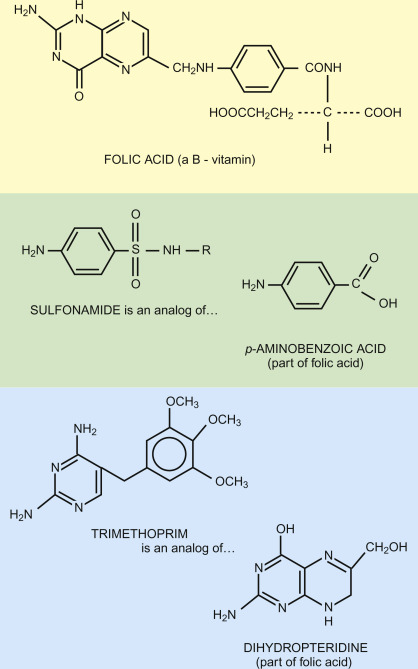
هيتشينجز واليون و فريقهم كمان كملوا شغل على ال Folic acid و الانزيم DHFR اللي كنا اتكلمنا عليه مع MTX الدوا . الفكرة برده انهم هيشتغلوا بنفس الطريقة و يحاولوا بطوروا مواد شبه الFolic acid عشان يكون عندها ارتباط قوي بالانزيم بس بشكل انتقائي في خلايا البكتريا أو الطفيليات مستغلين الفرق بين الانزيم البشري و مه في الكائنات الثانية ، و دا كان نتيجته انتاج Pyrimethamine اللي ارتباطه بالإنزيم في طفيل الملاريا اكثر من ٢٠٠٠ ضعف منه في الإنسان.
كمان Trimethoprim عنده ارتباط أعلى بـ100,000 مرة بالإنزيم البكتيري مقارنة بالإنزيم البشري. و بعدها تم اكتشاف إن التأثيرات العلاجية للدوا بتتزايد بشكل كبير مع مركبات السلفا اللي هي بتمنع تصنيع حمض الفوليك في خلايا البكتريا . المبدأ العلاجي ده استخدم في الأدوية المركبة زي Septrin اللي بتستخدم في علاج العدوى البكتيرية .
آخر محطة في انجازات اليون هتخلص بعد تقاعد مديرها Hitchings . لما الفريق اللي هي بتشرف عليه هيطور لأول مرة مادة Antiviral و Specific اسمها Acyclovir و اللي احنا عارفينه باسمه التجاري Zovirax.
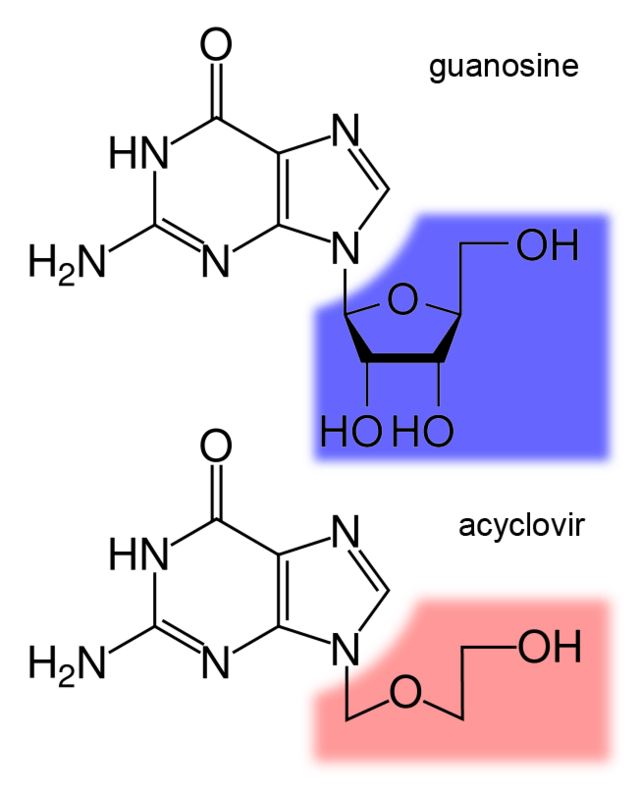
الفكرة هي نفسها بس هنطبقها في مكان تاني . المرة دي هنشوف خطوات بناء الDNA بتاع الفيروس وتكاثره وهنلاقيها هي هي تقريبا وباستخدام نفس المكونات . بس هنلاقي ان الانزيمات اللي موجودة مش واحدة . الفكرة ان احنا نطور مركب الفيروس يتعرف عليه و الخلية البشرية لأ . و هنا الفريق هيبتكر مركب له نفس شكل ال Nucleoside ال Guanosine يعني Base + Ribose . طبعا هنغيره عشان يمنع التكاثر و نشيل الribose و نحط مكانه جزئ تاني . الميزة في Acyclovir انه بيشتغل على انزيمات الفيروس بس من غير ما يكون له تأثير على خلايا الشخص المصاب . المميز انه خلايا الفيروس في البداية بتحول المادة بانزيم فيروسي اللي هو Thymidine kinase لشكل فعال . الشكل الفعال دا هيوقف انزيم الPolymerase الفيروسي برده يعني في كل الاحوال تأثيره انتقائي جدا .
نجاح Zovirax في حالات زي الجديري و الHerpes هيفتح شهية الفريق على استهداف انواع اخرى من الفيروسات ودا هيوصل في النهاية لأول Nucleoside reverse Transcriptase inhibitors أو NRTI لعلاج الايدز و اللي هو AZT او Ziduvudine و اللي معتمد على نفس الفكرة مع تعديل في التنفيذ . اللطيف ان AZT تمت اعتماده من الFDA بعد تقاعد اليون نفسها.
نجاح mercaptopurine و Azathioprine و Allopurinol و باقي الادوية اللي ذكرناها حفزت شركات كتير تسفيد من نفس الفكرة . شفنا مثلا شركة Roche بتعمل Mycofenolate أو Cellcept اللي برده بيعتمد نفس الطريقة وبيعطل انزيم في عملية الpurine metabolism عشان يستخدم برده في حالات زراعة الأعضاء .
كمان شركة Aventis و اللي اصبحت جزء من Sanofi استخدمت طريقة مشابهة لتطوير Leflunomide أو Avara /Arava اللي بيعطل برده Pyrimidine metabolism
و في الأورام في عدد ضخم من الأدوية اللي بتندرج تحت بند ال Antimetabolites زي 5FU و Xeloda و Fludara و غيرهم كتير.
خاتمة
في تاريخ جوايز نوبل للطب بيكون من النادر انه الفريق العلمي لشركة ادوية ياخد الجايزة . حالة اليون و هيتشيجنز كانت واحدة من الحالات النادرة دي . الجايزة ماكنتش بس بسبب الادوية اللي اخترعوها وبس . الجايزة بسبب تغيير طريقة تطوير الأدوية نفسها بشكل خلى انتاج ادوية مبتكرة لحالات كتير كان ميئوس من علاجها . ولما نضيف عليهم زميلهم الثالث اللي طور للمرة الأولى beta blocker و H2 blocker و كرس حياته لدراسة الReceptors هتلاقي ان التغيير اللي الناس دي سببته في عالم الادوية كان جذري و انهى بشكل نهائي الحاجة لانتظار الصدف .
Refrences
https://www.nobelprize.org/prizes/medicine/1988/summary/
https://www.mayoclinic.org/drugs-supplements/azathioprine-oral-route/description/drg-20067180
https://www.acs.org/content/acs/en/education/whatischemistry/landmarks/gertrudeelion.html
https://www.britannica.com/science/antimetabolite
https://www.sciencedirect.com/topics/medicine-and-dentistry/purine-metabolism
https://www.medscape.com/viewarticle/406854