Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124
Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة
مضادات الأيض Antimetabolites هي حجر الأساس في علاج كتير من أمراض المناعة الذاتية زي الذئبة الحمراء، التصلب المتعدد، والروماتويد. وبعد ظهور أزاثيوبرين في الخمسينات أزاثيوبرين في الخمسينات، حصل تطور كبير في أدوية المناعة الذاتية عشان نلاقي حلول أكتر أمانًا وفعالية. أدوية زي Cellcept – Mavenclad – Avara – Aubagio بقت خيارات مهمة، لكنها محتاجة متابعة دقيقة في ضبط الجرعات وتوعية المرضى. في المقال ده، هنحاول نعرف تاريخ الأدوية دي، آليات عملها، استخداماتها، جرعاتها ، ومخاطرها، مع نصائح عملية للصيادلة عشان يساعدوا المرضى بأمان.
الأزاثيوبرين (Imuran) زي ما اتكلمنا في موضوع سابقزي ما اتكلمنا في موضوع سابق كان خطوة كبيرة في علاج الأورام و أمراض المناعة الذاتية وزراعة الأعضاء ، بيشتغل عن طريق انه بيمنع تصنيع البيورينات اللي هي جزء رئيسي من بناء ال DNA ، وده بيقلل نشاط الخلايا سريعة الانقسام و منها الخلايا المناعية. لكن مشاكله زي تأثيره على نخاع العظم و سمية الكبد العالية وزيادة مخاطر الليمفوما خلّت العلماء يدوروا على بدائل أكتر أمانًا. ودا اللي هنتكلم عنه النهارده بالتفصيل
قصة ميكوفينوليت Mycophenolate تعتبر قديمة . المادة الفعالة mycophenolic acid تم استخلاصها في بداية القرن العشرين لأول مرة في من أحد الفطريات و تم دراستها كمضاد حيوي ولكن بسبب سميتها العالية تم اهمالها . ولكن في السبعينات رجع الاهتمام بيها لما طبيب جنوب أفريقي عمل ابحاث لاستخدامها بديل عن Azathioprine . و عشان يقلل السمية العالية استخدم ester بدل عن الحمض و عمل لنا ميكوفينوليت موفيتيل (CellCept) . الدوا ظهر في التسعينات في البداية لزراعة الأعضاء، وبعدين بقى خيار قوي في علاج الذئبة الكلوية والوهن العضلي لأنه أقل في كبت النخاع Bone marrow suppression من الأزاثيوبرين.
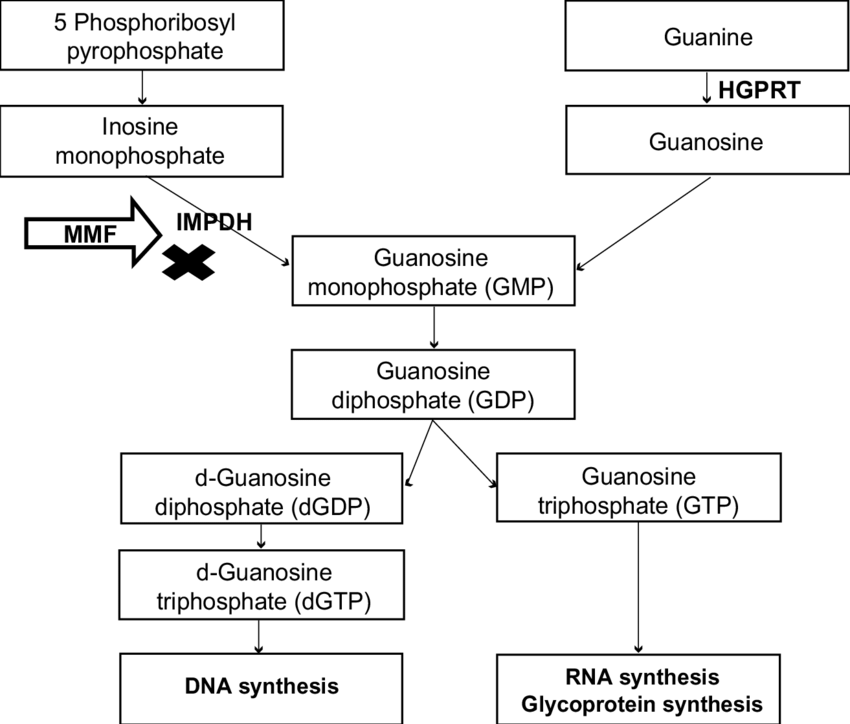
الخلايا بتقدر تصنع مكونات ال DNA بطريقتين : إما من مكونات أولية غي عملية اسمها De Novo synthesis أو من بقايا عضوية من خلايا ماتت مثلا في عملية اسمها Salvage pathway . أغلب خلايا الجسم تقدر تصنع احتياجاتها بالاعتماد على ال Salvage pathway. الخلايا سريعة الانقسام زي خلايا المناعة lymphocates بتعمد بالاساس على الDe Novo synthesis . ودا بيخلي استهداف المسار دا انتقائي للمناعة.
ميكوفينوليت MMF بيتحول الأول للحمض Mycophenolic acid اللي هو الشكل الفعال . آليه عمله بتعتمد على إنزيم اسمه IMPDH، ودا واحد من الانزيمات الأساسية لبناء Purines في مسار de novo . ميكوفينوليت بيمسك في الانزيم دا و يبطل مفعوله و بالتالي يقلل بناء الPurines و خاصة Guanosine ، الميزة هنا ان الدواء بيستهدف المناعة بدقة لان باقي الجسم بيتكيف عن طريف Salvage pathway
Cellcept بيستخدم في الحالات التالية :
الجرعات بتتقسم على جرعتين يوميا و بتتحسب على حسب الحالة وان كان اغلب الجرعات بتكون بين ١ و ٢ جم في الجرعة الواحدة . Cellcept موجود على شكل اقراص 500 مج ودا معناه ان المريض هيحتاج من قرصين ل ٤ في الجرعة حسب الحالة .
لو الكلى ضعيفة (GFR < 25 مل/دقيقة)، الجرعة لازم تقل . لازم يتاخد مع الأكل بنفس التوقيت عشان الامتصاص (72–94%).
بعد الCellcept شركة نوفارتيس نزلت نفس المادة بس مع اختلاف انه بدل استخدام الEster استخدموا ملح صوديوم و عملوا المركب مضاد للتحلل في المعدة Enteric coated . المنتج الجديد نزل في أول الألفية باسم Myfortic . الفروق على مستوى النتايج بين Cellcept و Myfortic مش ضخمة

المادة الثانية من مضادات الايضAntimetabolites اللي هنتكلم عنها هي ليفلونوميد Leflunomide . الدوا اللي طورته شركة Aventis – جزء من سانوفي حاليا اتوافق عليه سنة 1998 لعلاج الروماتويد، ولكن على عكس Azathioprine و Mycofenolate ف Leflunomide هيشتغل على تصنيع البيريميدينات pyrimidines مش الPurines . القواعد الثانية في تصنيع الDNA
ليفلونوميد بيمنع إنزيم اسمه DHODH، الانزيم دا له دور اساسي في تصنيع uridine monophosphate، وده Pyrimidine و عنصر أساسي في الحمض النووي والـRNA في طريق ال De Novo synthesis . و بشكل مشابه للي اتكلمنا عنه في cellcept فالدواء بيقلل تكاثر خلايا T وB المناعية .
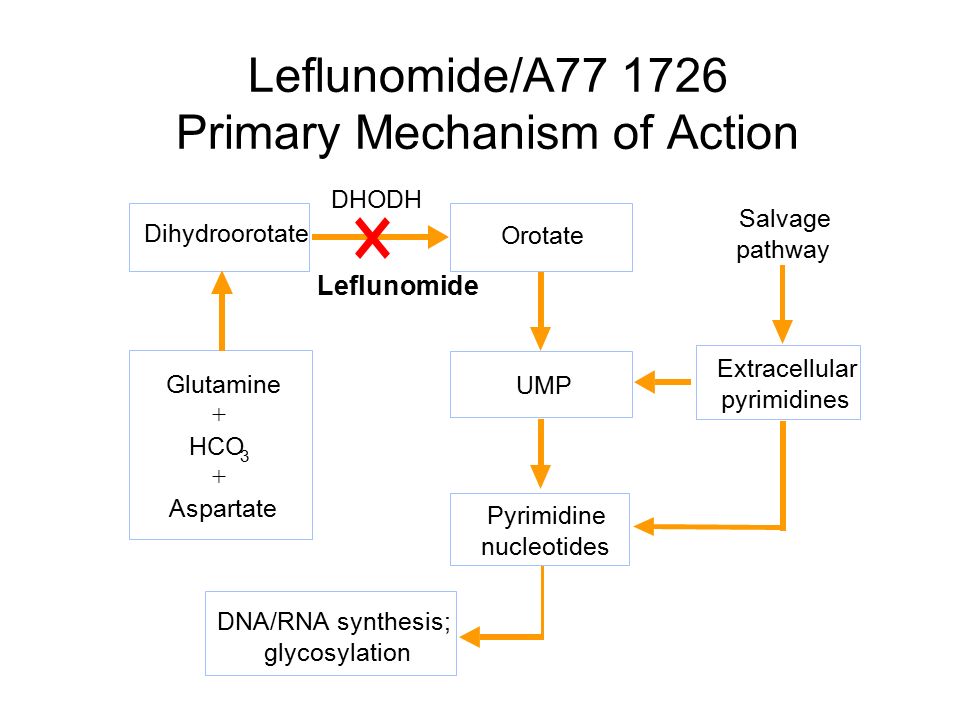
الاختلاف المهم هنا هو انه Leflunomide بالاضافة لدوره في منع تصنيع الDNA , كمان بيوقف تتابعات التهابية مسؤول عنها نفس الانزيم . و بالتالي فله أثر مضاد للالتهابات زائد تأثيره المناعي
دا وجه التجارب السريرية انها تركز على استخدامه في علاج الروماتويد بالاساس و بخاصة لما المريض ما يستجبش بشكل كافي مع Methotrexate لوحده أو يكون ماينفعش يستخدمه :
– جرعة ليفلونوميد :في البداية جرعة Loading Dose كبيرة ١٠٠مجم/يوم لمدة 3 أيام، و بعد كدا 10–20 مجم/يوم.
– في التهاب المفاصل المصاحب للصدفية : 10 مجم ممكن تكفي.
– التأثير بيظهر خلال 6–12 أسبوع.
>تأثير الدوا طويل جدا ال Halflife بيوصل ل (~14 يوم) ودا معناه مفعول طويل ودائم ، بس كمان معناه انه بيتراكم في الجسم وممكن آثاره الجانبية تزيد بالوقت ، فمحتاج متابعة دقيقة.
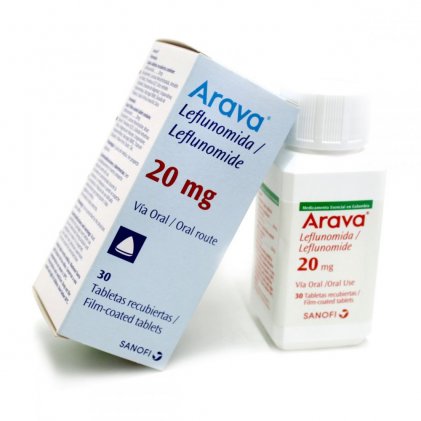
الآثار الجانبية زي إسهال (~20%)، طفح جلدي، وتساقط الشعر من مخاطر ليفلونوميد.
سمية الكبد من المشاكل المهمة و محتاجة تحاليل كل 3–4 شهور.
الدواء مُشوّه للجنين، ولازم يتوقف قبل الحمل بفترة طويلة .
في امكانية للتخلص من السمية و غسيل الجسم من المادة عن طريق استخدام الـcholestyramine
اعتمادا على نجاح ليفلونوميد تم تطوير ال Active metabolite له Teriflunomide بس المرة دي لاستخدام مختلف و هو MS ، اتوافق عليه سنة 2012 المرة دي لعلاج التصلب المتعدد (RRMS) بطريقة أكتر دقة. بس طبعا دا وفر مصدر دخل جديد للشركة بعد ما فترة براءة اختراع Leflunomide خلصت
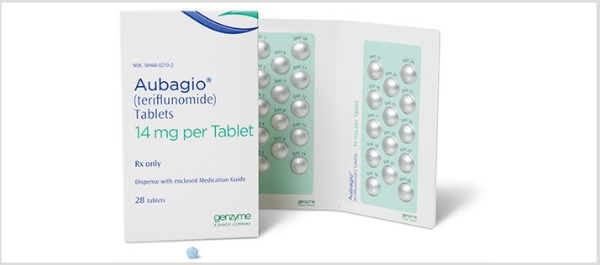
المادة الفعالة الأخيرة معانا النهاردة من الAntimetabolites مختلفة كتير عن اللي فاتوا . كلادريبين اتطور في البداية التمانينات لعلاج سرطانات الدم، وبعدين توسع استخدامه في علاج التصلب المتعدد (RRMS) في الألفينات، ورغم ان الWHO حطته على قايمة الأدوية الأساسية لعلاج الMS إلا انه لسه مش بيتوصف كتير بسبب القلق من آثاره الجانبية و بيتم الاستعانة به للحالات المستعصية لما الأدوية الفموية التانية سواء Aubagio أو Gilenya & Tecfidera تكون مش كافية .
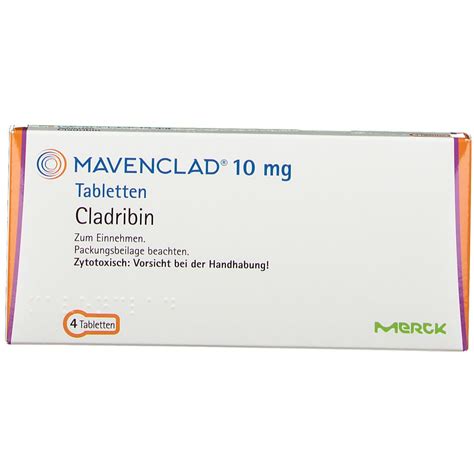
الكلادريبين مش بيشتغل على الDe novo Sythesis .لا دا شغال على العملية المضادة . الخلايا بعد ما بتصنع مايكفيها من الPurines و ال Pyrimidines لعمل الDNA بتكسر الباقي . أحد الانزيمات الأساسية في عملية الهدم هو انزيم Αdenosine deaminase . الانزيم دا مسؤول بالاساس عن تكسير الPurine اللي اسمه Adenosine . الفكرة من Cladibrine انه يكون شبه الAdenosine مع اختلاف انه مش هيتكسر من الdeaminase . بالتالي مع الوقت هيتراكم في الخلايا وبيدمر الحمض النووي، سواء في الخلايا النشطة أو الراكدة، وده بيقلل عدد اللمفاويات لفترة طويلة.. انزيم Adenosine deaminase موجود بالاساس في الخلايا المناعية و دا بيخلي لل Cladribine انتقائية الى حد ما .
دا بيخلي Cladribine فعال في اورام الدم الناتجة عن زيادة انقسام الخليا B-cells و دا اللي كمان خلاه خيار ممتاز للMS . حتى اقوى من Aubagio للحالات الشديدة أو اللي المرض بيتطور فيها بسرعة و بيقلل معدل النوبات بنسبة 50% .
بتتقسم على سنتين ( بيتاخد 10–20 مجم/يوم لمدة 4–5 أيام في الشهر الأول والثاني من كل سنة لمدة سنتين ).
لازم قبل كل دورة نتأكد إن مفيش عدوى نشطة وإن عدد الخلايا المناعية عالي أو مستواه طبيعي
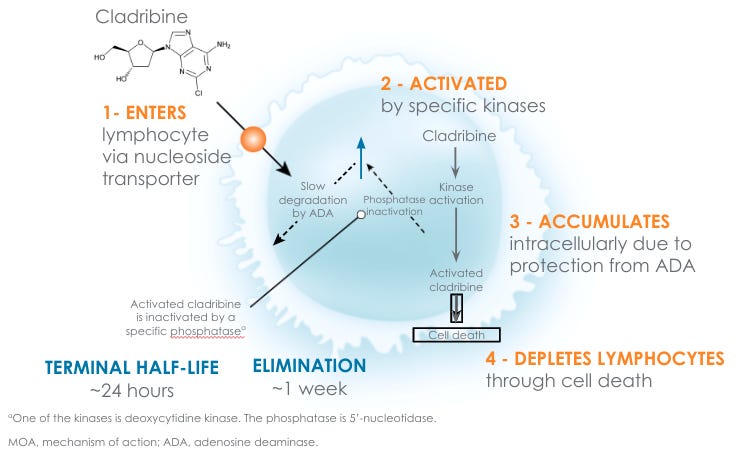
مخاطر كلادريبين تشمل نقص الخلايا الليمفاوية زيادة العدوى، وفيه احتمال لتطور انواع سرطانات تانية. الدواء مُشوّه للجنين، فلازم منع حمل. الصيادلة ينصحوا بمتابعة مستمرة للعدوى وتحذير المرضى من أي علامات خطر.
مضادات الأيض Antimetabolites زي ميكوفينوليت موفيتيل. كلادريبين، ليفلونوميد، وتيريفلونوميد بتقدم حلول متقدمة لعلاج أمراض المناعة الذاتية زي الذئبة الحمراء التصلب المتعدد، والروماتويد. كل دواء بيستهدف مسار معين في المناعة، لكن محتاج متابعة . ضروري متابعة تحاليل الدم والكبد، وتوعية المرضى بمخاطر سمية الكبد والتأثير على الحمل .
المراجع:
– Mycophenolate vs. Azathioprine in Lupus Nephritis: New England Journal of Medicine, 2011
– Teriflunomide in MS: PMC, www.ncbi.nlm.nih.gov
– Leflunomide Safety Profile: ResearchGate, 2020
– Cladribine in MS: PMC, www.ncbi.nlm.nih.gov