Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124
Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

Kortison, oder allgemein Glukokortikoide, gehören zu den wichtigsten Medikamenten in der modernen Medizin. Sie wirken stark und zuverlässig: bei Allergien, Entzündungen, Rheuma, Autoimmunerkrankungen, bei Krebs und sogar bei Organtransplantationen. Heute nehmen etwa 1–2 % der Weltbevölkerung dauerhaft Glukokortikoide gegen chronische Krankheiten ein. Noch mehr Menschen bekommen sie vorübergehend bei akuten Beschwerden.
Das sind sehr große Zahlen – und trotzdem haben viele Menschen Angst vor Kortison, wegen der Nebenwirkungen. Aber die Wahrheit ist: Wenn Kortison richtig und in passender Dosierung eingesetzt wird, kann es Leben retten und die Lebensqualität deutlich verbessern. Der Schlüssel liegt im genauen Verständnis, wie es wirkt und wie man die Nebenwirkungen kontrolliert.
Glukokortikoide wirken nicht nur oberflächlich auf Symptome – sie greifen tief in die Zellen und Gene ein. Genau das macht sie so stark. In diesem Artikel schauen wir uns die Geschichte des Kortisons an – von der Entdeckung bis zu seiner heutigen Rolle – und wie es das Leben vieler Patienten verändert hat.
Früher galt die Nebenniere (die Drüse oberhalb der Niere) als unwichtig. Im 19. Jahrhundert entfernten Forscher die Nebenniere bei Versuchstieren – und die Tiere starben. Da wurde klar: diese Drüse muss lebenswichtig sein, aber niemand wusste warum.
Der englische Arzt Thomas Addison (nicht der mit der Elektrizität!) beobachtete Mitte des 19. Jahrhunderts Patienten mit sehr merkwürdigen Symptomen: extreme Schwäche, ständige Müdigkeit, Gewichtsverlust, dunkle Hautverfärbungen und extrem niedrigen Blutdruck.
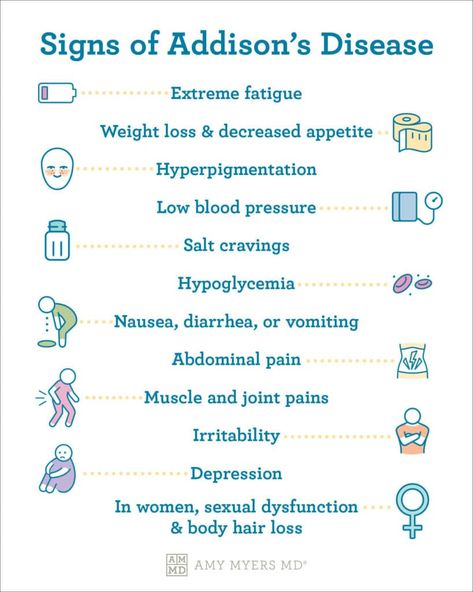
Nach Untersuchungen stellte er fest, dass diese Patienten zerstörte Nebennieren hatten. Er beschrieb die Krankheit, die wir heute Morbus Addison nennen. Damit war klar: die Nebenniere hat eine wichtige Funktion – aber welche genau, wusste man damals noch nicht.
In den 1930er Jahren versuchte der Biochemiker Edward Kendall an der Mayo Clinic in den USA die Stoffe der Nebenniere zu isolieren. Das war schwer, weil die Drüsen winzig sind und die Hormone nur in Spuren ausgeschüttet werden.
1936 gelang es Kendall, mehrere Stoffe zu isolieren. Zwei davon hießen „Compound E“ und „Compound F“ – später bekannt als Kortison und Kortisol (Hydrokortison).
Das war ein riesiger Durchbruch: Kendall entdeckte, dass Kortison den Stoffwechsel und Entzündungen beeinflusst – der Grundstein für seine spätere medizinische Nutzung.
In den 1940er Jahren arbeitete der Rheumatologe Philip Hench ebenfalls an der Mayo Clinic. Er hatte beobachtet, dass Patienten mit Rheumatoider Arthritis manchmal plötzlich besser wurden, z. B. während einer Schwangerschaft. Er vermutete, dass ein Hormon dafür verantwortlich sei.
Hench begann mit Kendall zusammenzuarbeiten und testete Compound E (Kortison) bei Patienten.
1948 bekam eine 29-jährige Frau mit schwerem Rheuma erstmals Kortison. Wenige Tage später konnte sie wieder laufen und ihre Hände bewegen – fast ohne Schmerzen. Das Ergebnis wirkte wie ein Wunder.
Das löste den weltweiten „Cortisone Boom“ aus. 1950 erhielten Kendall, Hench und ein weiterer Forscher den Nobelpreis für Medizin.
Schon früher hatte der Schweizer Chemiker Leopold Ruzicka (Uni Zürich, Nobelpreis 1939) gezeigt, dass viele Hormone mit Cholesterin verwandt sind. Diese nannte er Steroide – sie haben eine Grundstruktur aus 4 Kohlenstoffringen. Er beschrieb zum Beispiel das männliche Hormon Testosteron.
Sein Schüler Tadeus Reichstein erforschte die Nebenniere und zeigte, dass Kendalls „Compound E und F“ ebenfalls Steroide sind – abgeleitet vom Cholesterin. Da sie aus der Rinde (Cortex) der Nebenniere stammen, heißen sie Kortikosteroide.
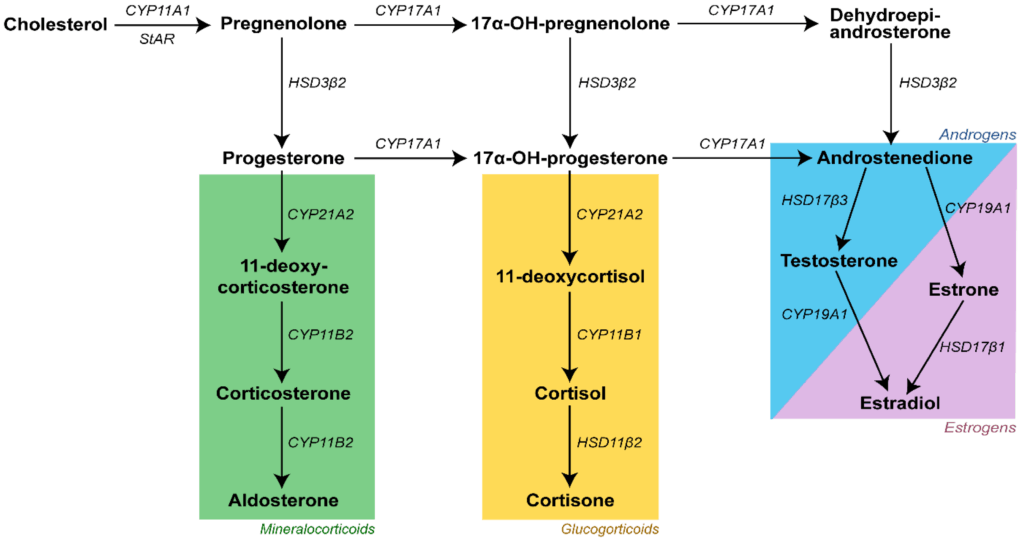
Reichstein erklärte auch die chemische Struktur und den Stoffwechsel von Kortison/Kortisol. Dafür erhielt er 1950 zusammen mit Kendall und Hench den Nobelpreis. Sein Wissen machte später die industrielle Herstellung von Kortison möglich.
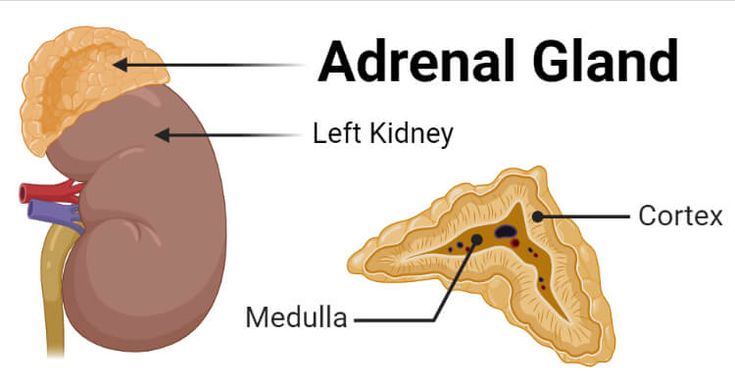
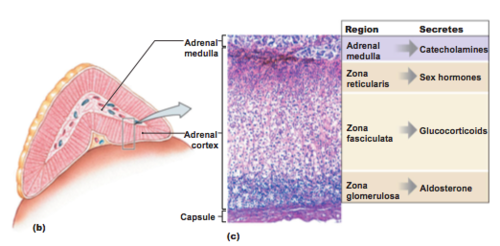
Die Nebennierenrinde produziert zwei Hauptarten von Steroidhormonen:
Im Inneren der Nebenniere (Mark) wird dagegen Adrenalin gebildet – kein Steroid.
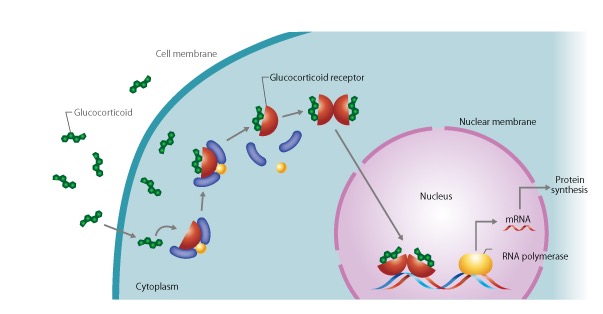
Kortison wirkt, indem es sich an spezielle Glukokortikoid-Rezeptoren in fast allen Körperzellen bindet. Diese sitzen im Zellinneren. Nach Bindung gelangt der Komplex in den Zellkern und verändert die Genaktivität:
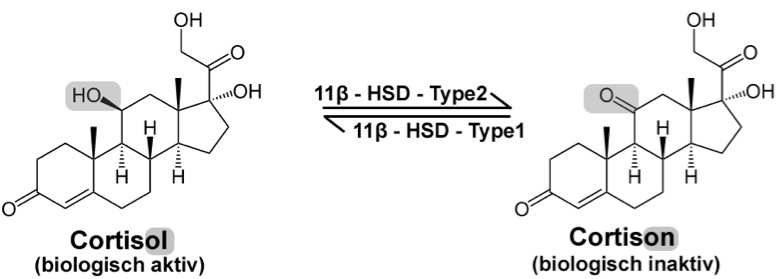
Kortisol ist dabei die aktivste Form, aber kurz wirksam. Der Körper wandelt es teilweise in inaktives Kortison um und aktiviert es bei Bedarf wieder.
Anfangs war Kortison extrem teuer, weil man es aus tausenden Nebennieren von Rindern gewinnen musste.
Der Chemiker Russell Marker fand eine Lösung: Im mexikanischen Wild-Yam (Dioscorea) steckt die Substanz Diosgenin, die chemisch dem Kortison ähnelt.
Marker entwickelte ein Verfahren, daraus Kortison herzustellen, und gründete die Firma Syntex in Mexiko. Das senkte die Kosten drastisch und machte Kortison für viele Patienten verfügbar. Später kaufte Roche die Firma.
In den 1950er Jahren entwickelte Arthur Nobel (Firma MSD) stärkere und nebenwirkungsärmere Kortison-Abkömmlinge:
Damit konnten Ärzte Kortison sicherer bei Asthma, Darmentzündungen oder Lupus einsetzen.
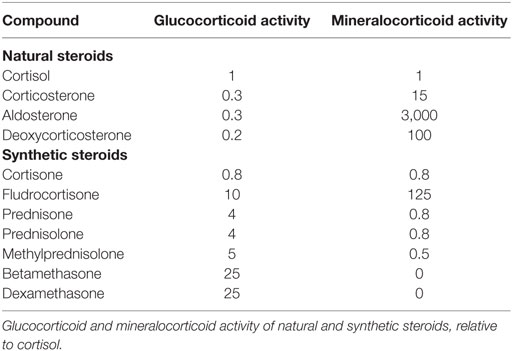
In den 1960er Jahren kamen noch stärkere Glukokortikoide auf den Markt, z. B.:
Sie sind etwa 25-mal stärker als Kortison, wirken länger und ohne Einfluss auf den Salzhaushalt. Man nutzt sie bei akuten Notfällen, Autoimmun-Schüben, bestimmten Krebserkrankungen.
2020 spielte Dexamethason eine Schlüsselrolle in der COVID-19-Therapie, da es schwere Lungenentzündungen dämpfte und Sterblichkeit senkte.
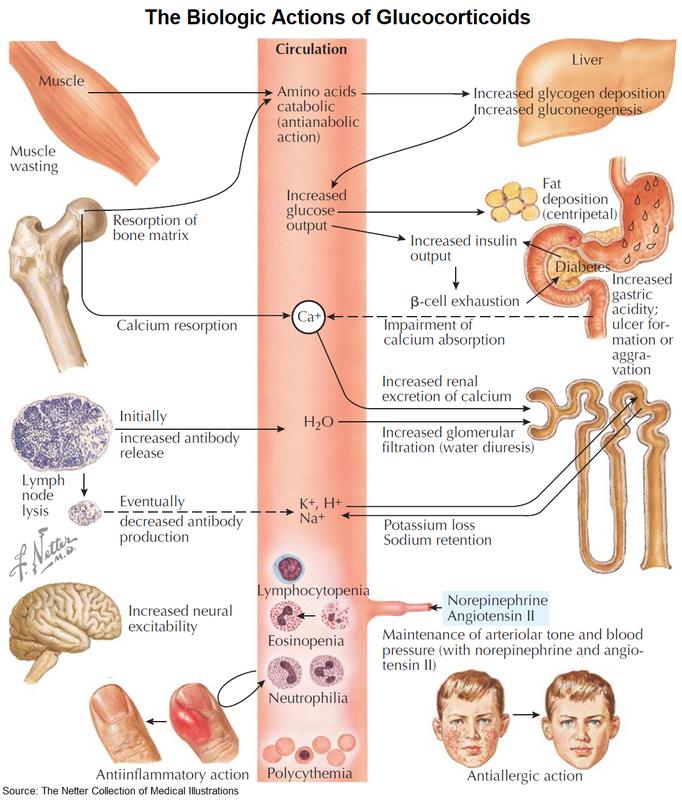
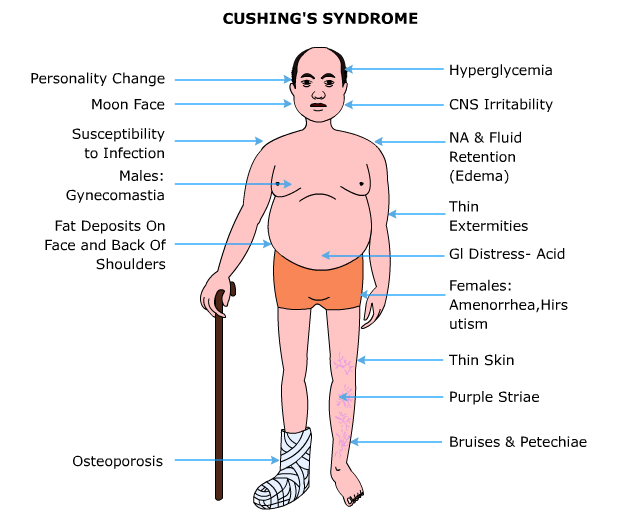
Wenn der Körper zu viel Kortisol produziert (z. B. durch Tumoren) oder der Patient zu lange hohe Dosen Kortison einnimmt, entsteht Morbus Cushing:
Behandlung: Operation bei Tumoren oder langsames Ausschleichen der Medikamente.
Die Entdeckung des Kortisons hat die Medizin verändert – von Addison bis heute. Dieses Hormon ist ein mächtiges Werkzeug gegen viele Krankheiten. Ja, es hat Nebenwirkungen, aber bei richtiger Anwendung überwiegt der Nutzen deutlich.
Die Zukunft bringt wahrscheinlich noch gezieltere Medikamente, die wirksamer sind und weniger Risiken haben – sodass Kortison weiterhin Millionen Leben retten kann.