Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124
Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

تعليم دوائي مستمر بأسلوب مبسط للصيادلة و المهتمين بالمعرفة

لحد سنة 2010 كان علاج التصلب المتعدد Μultiple Sclerosis الوحيد هو الحقن بالإنترفيرون أو حقن أخرى في حالات قليلة . ولكن في سنة 2010 تم اعتماد أول دوا أقراص بالفم للمرض وهو Gilenya من شركة Novartis واللي بيحتوي على مادة Fingolimod .ورغم نجاحه الكبير الا ان بعض الاثار الجانبية كانت مخوفة المرضى و الاطباء بالذات في البداية . بعدها ب٣ سنين وفي ٢٠١٣ نزل دوا ثاني برده أقراص بالفم من شركة Biogen اسمه Tecfidera و بيحتوي مادة Dimethyl fumarate وعمل طفرة ثانية . المادتين دول غيروا طريقة علاج التصلب المتعدد و قللوا الاحتياج للحقن . حاليا الادوية الفموية أصبحت هي الخط الأول في أغلب خطط العلاج . النهارده هنحاول نعرف اكتر عن المادتين دول ومميزات و عيوب كل واحد فيهم.

البداية ملخص سريع عن المرض : الخلايا المناعية بتبدأ تهاجم الغشاء الواقي للخلايا العصبية Myelin Sheath . الهجوم دا بيؤثر على نقل الاشارات العصبية و بيتسبب في نوبات من الاعراض بتستمر لاكثر من يوم . الاعراض بتكون اضطراب في الحركة و النظر و السمع و الاتزان و خلل في الوعي و الادراك و صعوبة في التفكير و التركيز . التشخيص بيعمد بالأساس على الاشعة و اللي بتوضح ندبات او مناطق فيها تلف في المخ و الحبل الشوكي بسبب عدم وجود طبقة الوقاية على الاعصاب .
المرض ليه ٤ أنواع فرعية مختلفة حسب نمط الاعراض و هل بيرجع المريض بعد النوبات طبيعي و لا بتأثر عليه و ازاي بيتطور المرض الوقت . الانواع دي بيوضحها الشكل اللي جاي دا . النوع الأكثر شيوعا هو الRelapsing remitting ودا بيمثل تقريبا ٨٥٪ من الحالات . و الادوية اللي هنتكلم عنها النهارده بتساعد في النوع دا . باقي الأنواع ليها أدوية أخرى أتكلمنا عنها قبل كده هنا وهنا
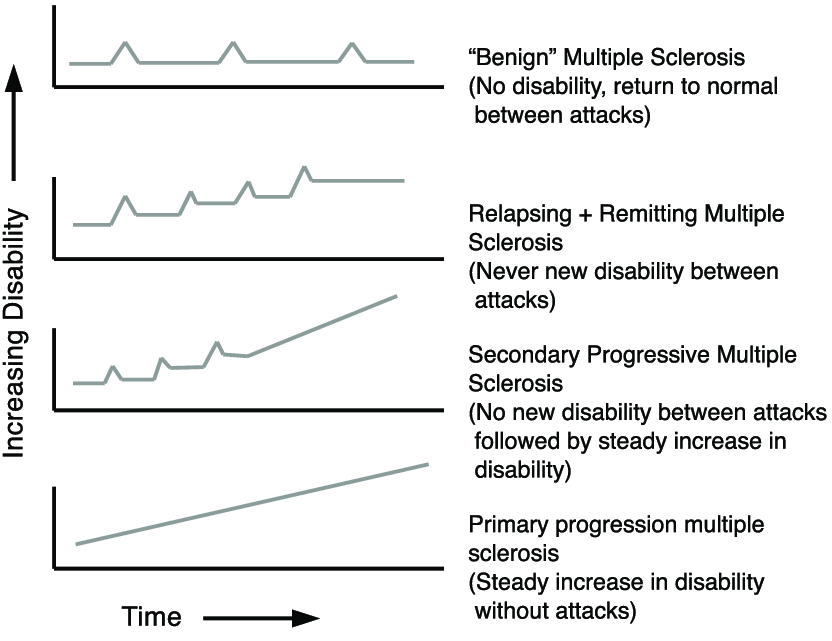
المرض التوعية بيه مش كبيرة في الشرق الأوسط وفي مرضى بتعيش بيه من غير علاج ومن غير ماتفهم هم عندهم ايه . في امريكا و اوروبا وشرق اسيا الاهتمام بالمرض اعلى و المسح عنه اكثر و بالتالي بيتم اكتشافه اكتر . وان كان في دراسات قالت ان المرض اصلا منتشر اكتر في المناطق الباردة و بين اصحاب بعض الاعراق.
العلاج بيكون هدفه تقليل الاعراض و كمان تقليل حدوث الاعراض و تقليل فرصه تطور المرض .بدون علاج ممكن لا قدر الله يتطور المرض الى فقد للبصر او شلل أو تشنج عضلي . المريض بياخد بجانب الادوية اللي بتعالج الاعراض نفسها ادوية تأثر على المناعة و تكون Disease Modifying . زي ما اتكلمنا قبل كدا فأولها الأدوية المستخدمة كان ال Interferon beta . لحد ما ظهر ابطال النهارده وخلينا بقى نتكلم عنهم بشكل مفصل و نبدأ بGilenya
في اواخر القرن ال١٩ و في اثناء تحليل المواد العضوية تم اكتشاف مواد دهنية موجودة في الدم و مختلفة عن الكوليسترول و الدهون الثلاثية . الدهون دي تم تسميتها على اسم ابو الهول بتاعنا Sphinx نظرا لغموض دورها وقتها و بالتالي سموها Sphingosine Lipids . بالوقت عرفنا انهم بيدخلوا في بناء الغشاء Plasma Membrane اللي موجود في كل الخلايا الحية . بعدها عرفنا انه ليه اكتر من نوع واهمهم هو ال Ceramide وانه بيتم صناعته داخل الخلية .
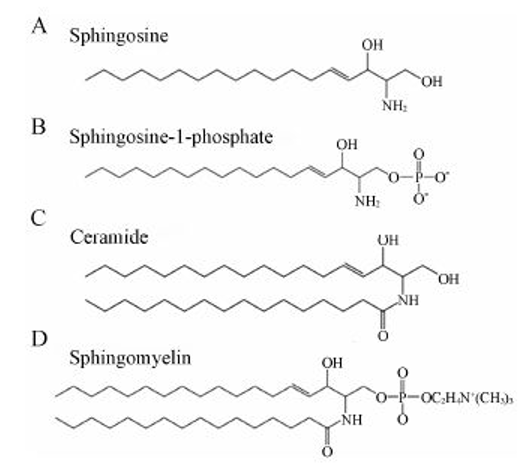
وفي إطار الابحاث عن الSphingosine تم استخلاص مادة شبه الSphingosines من احد الفطريات . المادة دي اسمها myriocin و لقينا ان ليها اثار مضادة للمناعة . و عشان نقلل السمية ونحسن التأثير بدأ الباحثين يغيروا في تركيب المادة لحد ما طلعتلنا مادة Fingolimod . وبرغم من فعاليتها الا ان آليه عملها فضلت لفترة مش قصيرة تحت الدراسة لحد ما تم توضيحها فتعالوا نعرف
خلونا نرجع للPlasma Membrane و الceramide و مع النمو او عند موت الخلية بيتم تكسير الCeramide اللي في جدار الخلية . بعدها بيتحول في وجود انزيمات لأكتر من نوع مختلف من الSphingosines واحد منهم هو Sphingosine -1 Phosphate أو S1P ودا بيكون تواجده في الدم خارج الخلايا ورفي الأغلب مرتبط ببروتينات .
S1P انه ليه ادوار تانية خالص غير دور الCeramide . دا لأنه ليه مستقبلات S1P Receptors على سطح خلايا كتير في الجسم . تفاعل S1P مع مستقبلاته له ادوار كتير و تأثيرات كتير لسه بنفهمها كلها لحد الآن . احنا دلوقتي نعرف ٥ انواع من المستقبلات ل S1P اهمها على الخلايا المناعية و العصبية و القلب و الأوعية الدموية .
الS1P ليه مستقبلات على خلايا الLymphocytes زي الT-cells و الB-cells . ولما الS1P يمسك في المستقبل بتاعه على الخلايا دي بيوجه حركة الخلية من العقد الليمفاوية للدم عشان الجسم يوديها مكان العدوى أو الخطر
آلية عمل Fingolimod او Gilenya تعتمد على تفاعله مع مستقبلات S1P على الخلية الليمفاوية بشكل دائم Irreversible ، ودا بيؤدي إلى احتباس الخلايا المناعية داخل العقد اللمفاوية، وبالتالي تقليل انتقالها إلى الدم و منه الى الجهاز العصبي المركزي (CNS). دا بدوره بيمنع الخلايا المناعية من مهاجمة غشاء الميالين، و بيقلل من الالتهاب والنوبات. فينجوليمود بالتالي يعتبر أول S1P receptor modulator.
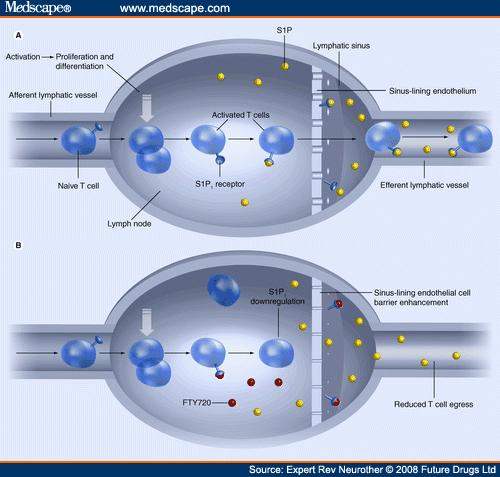
كمان، مستقبلات الS1P موجوده على سطح الخلايا العصبية و تنشيطها هنا له دور في نمو الخلايا و تمايزها و تطورها و بالتالي بما انه فينجوليمود بيتميز بقدرته على عبور (Blood-Brain Barrier) بسبب طبيعته الدهنية فدا بيسمح له بالتأثير مباشرة على الخلايا العصبية في الدماغ. دراسات على نماذج حيوانية، أظهرت إن الفينجوليمود ممكن يساعد على حماية الخلايا العصبية وإصلاح الأضرار ، وده بيضيف تأثير عصبي واقي (Neuroprotective) محتمل بجانب تأثيره المناعي. ودا ممكن يكون السبب لتحويل مجرى الابحاث من حالات زراعة الأعضاء لعلاج التصلب المتعدد
في التجارب فينجوليمود أو جيلينيا قلل معدل النوبات السنوية بنسبة حوالي 54-60% مقارنة بال(Placebo)، وكمان قلل عدد Lesions الجديدة .
سهولة استخدامه على شكل اقراص بتستخدم مرة واحدة في اليوم و نجاحه الكبير ساعد في انتشاره برغم سعره الغالي وقتها و شجع على التوسع في دراسة ال S1P و مستقبلاته و المواد اللي بتأثر عليهم ودراسة امكانية استخدامهم في حالات مناعية تانية زي ما شوفنا بعد كدا مع Ozanimod او Zeposia اللي تم اعتماده كمان لالتهابات القولون
ولكن طبعا مفيش دوا مالوش آثار جانبية الفينجوليمود بيأثر كمان على مستقبلات الS1P اللي موجوده في القلب و بيسبب انخفاض مؤقت في معدل ضربات القلب (Bradycardia) أو تباطؤ في التوصيل الكهربائي للقلب (AV block). عشان كده، لازم يتم مراقبة المريض لمدة 6 ساعات على الأقل بعد الجرعة الأولى، مع قياس ضغط الدم وتخطيط القلب (ECG). المرضى اللي عندهم تاريخ أمراض قلبية زي النوبات القلبية أو قصور القلب لازم يتجنبوا الدواء إلا لو كان عندهم جهاز تنظيم ضربات القلب.
وطبعا بما إن الفينجوليمود بيقلل عدد الخلايا اللمفاوية اللي بتوصل الى الدم هيبقى بيزيد مخاطر العدوى. العدوى تشمل هنا التهابات الجهاز التنفسي أو عدوى الفيروسات زي ال Herpes بانواعها او في حالات نادرة كمان فيروس PML . عشان كده، لازم يتم فحص صورة الدم (CBC) قبل وأثناء العلاج و يفضل المريض يكون واخد تطعيم ضد الHerpes Zoster .
بالاضافة للي فات فمستقبلات S1P ليها دور في الangiogenisis في العين . الفينجوليمود بتعطيله لعملها ممكن يسبب تورم في شبكية العين، مما يؤثر على الرؤية. المرضى اللي عندهم تاريخ التهاب القزحية أو السكري أكثر عرضة، وبالتالي لازم يعملوا فحص عيون دوري.
وأخيرا Gilenya ممكن يسبب مشاكل الكبد (زيادة إنزيمات الكبد)، وفي حالات نادرة سرطانات الجلد.
جيلينيا ممنوع في السيدات الحوامل او اللي بيفكروا يحملوا . ده لأنه ممكن يسبب تشوهات للجنين بسبب دور ال S1P في نمو وانقسام الخلايا و الAngiogenesis . اتكلمنا عن المشكلة دي مع الThalidomide.
كمان لو المريض هيوقف جيلينيا، لازم يكون تحت إشراف طبي . ده لأن إيقاف الدواء فجأة ممكن يسبب تفاقم شديد لأعراض التصلب المتعدد، وده بيسموه Rebound Effect
المشاكل دي خلت جيلينيا مش مناسب لمرضى كتير . بالتالي كان في حاجة لخيار تاني بالفم للحالات دي . الحل دا ظهر بعدها ب٣ سنين و اسمه Tecfidera . تعالوا نحكي حكايته هو كمان.
قصة Tecfidera بدأت في ألمانيا في الخمسينيات. وقتها، العالم الألماني والتر شفيكينديك (Walter Schweckendiek) كان مصاب بالصدفية (Psoriasis). وفي بحثه عن علاج افترض إن الصدفية ممكن تكون ناتجة عن خلل في دورة حمض الستريك (Krebs Cycle).
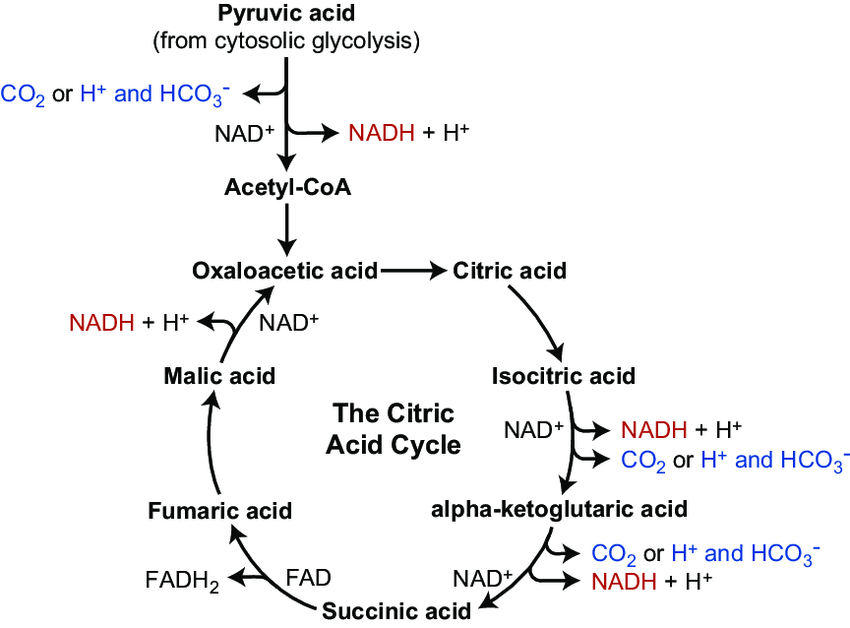
افتراضه خلاه قرر يجرب يعالج نفسه بالمواد الوسيطة في الدورة زي حامض (Fumaric Acid) ، لكن لقى إن حامض الفوماريك نفسه مش بيتم امتصاصه كويس في الأمعاء. فبدأ يشتغل على مشتقاته و خاصة الEsters و فعلا ظهرت نتايج مبشرة. بعد فترة ، تم تطوير دواء يُسمى Fumaderm في ألمانيا، وهو مزيج من Dimethyl Fumarate وإسترات أخرى واستخدم لعلاج الصدفية المتوسطة إلى الشديدة. الدواء ده كان ناجح جدًا في تقليل الالتهاب في الصدفية . و لكننا كنا فهمنا ان المرض مالوش علاقة بالKrebs cycle اصلا وان المرض و الدوا لهم علاقة بالمناعة .كمان كنا عرفنا ان مش كل الEsters ليها فعالية وانما فقط Dimethyl fumarate .
وهنا شركة Biogen اللي اصلا بتنتج الانترفيرون Avonex هيفكروا في تجربة Dimethyl fumarate على التصلب المتعدد و هيعملوا دراسات مستفيضة عن تأثيراته المناعية . بعدها يستحوذوا على الشركة اللي بتنتج Fumaderm . و هيبدأوا أول دراسة مفتوحة (Open-Label) على مرضى التصلب المتعدد باستخدام Fumaderm واللي أظهرت نتايج إيجابية. ولتحسين المفعول هيتم انتاج صيغة ممتدة المفعول (Delayed-Release) من Dimethyl fumarate لوحده تحت اسم Tecfidera، اللي أثبت فعاليته في التجارب وتم اعتماده من الFDA.

تعالوا نبعد عن المناعة و نروح للخليه العصبية اللي المناعة دلوقني بتهاجمها هنلاقيها واقعة تحت ما يسمى بالOxidative Stress اللي بيؤدي الى موتها و تدميرها . بس الخلية دي عندها سلاح ممكن تستخدمه للدفاع عن نفسها وهو مضادات الاكسدة اللي هي ممكن تفرزها . مضادات الأكسدة دي بتحتاج عشان تتفرز بروتين من عوامل النسخ Transcription factor يروح يمسك في الDNA و يحفز انتاج مضادات الأكسدة دي . الtranscription factor دا اسمه Nuclear factor erythroid 2-related factor 2(NRF2) . عامل النسخ NRF2 هو نفسه بيتم التحكم فيه عن طريق بروتين تاني اسمه Keap1 – البروتين دا ضروري لانه احيانا بيكون الجسم محتاج يتخلص من الخلايا و مش عايز الخلية تدافع عن نفسها.
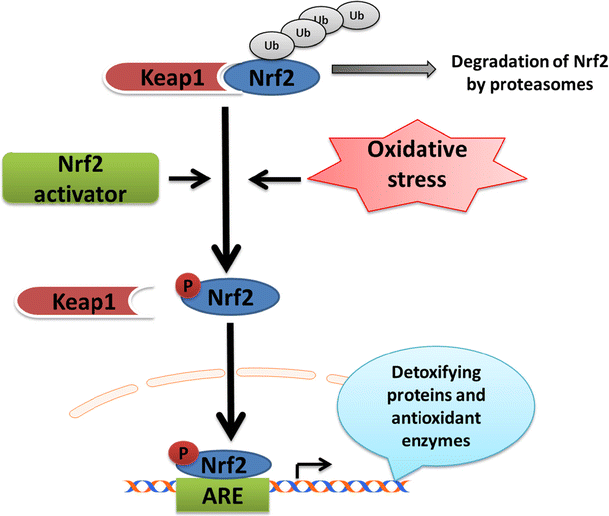
اهو Dimethyl fumarate او Tecfidera بيمسك في الKeap-1 تمام بفضل تركيبته الكيميائية و بيعطله . بالتالي NRF2 هيقدر يحفز انتاج مضادات اكسدة تحمي الخليه من هجوم المناعة.
غير التأثير دا ففي دراسات لقت علاقة قوية بين Dimethyl fumarate و بين نقص انتاج بعض البروتينات في الخلايا المناعية زي مثلا Integrin α4 المهم في التصاق الخلايا المناعية بالخلية العصبية . ودراسات تانية لقت نقص في عدد الخلايا المناعية و نقص في نشاطها . بس نقدر نقول ان التأثيرات المختلفة لTecfidera مش كلها واضحة
في التجارب السريرية، التيكفيديرا قللت معدل النوبات بنحو 44-50% مقارنة بالplacebo . كمان قللت عدد الآفات lesions الجديدة في الرنين المغناطيسي وأبطأت تطور الإعاقة . وبعد نزوله نجاحه في السوق كان ضخم جدا وخاصة بسبب آمان استخدامه مقارنة بالمنافسين . و استمر لفترة طويلة كأنجح دوا انتجته Biogen . النجاح دا كمان خلى الشركة تزود دراسات عشان تنزل نسخة أفضل منه عبارة عن Prodrug اقل في الآثار الجانبية . الProdrug نزل باسم Vumerity سنة ٢٠١٩
اقراص Tecfidera بشكل عام بتكون آمنة، لكن زيها زي أي دواء، ليها آثار جانبية، أهمها:
• التهابات الجهاز الهضمي: زي الغثيان، الإسهال، وآلام البطن، ودي بتكون أكتر شيوعًا في الأسابيع الأولى من العلاج. تناول الدواء مع الطعام أو البدء بجرعة منخفضة (120 ملجم مرتين يوميًا لأول 7 أيام) بيقلل الأعراض دي.

• الاحمرار (Flushing): إحساس بالحرارة أو احمرار الجلد، وده بيحصل عند حوالي 40% من المرضى. تناول الأسبرين قبل الجرعة ممكن يساعد في تقليل العرض دا.
• نقص الخلايا اللمفاوية (Lymphopenia): التيكفيديرا بتقلل عدد الخلايا اللمفاوية في الدم . عشان كده، لازم يتم مراقبة صورة الدم كل 6-8 أسابيع في السنة الأولى.
• مشاكل الكبد: زيادة إنزيمات الكبد، وده بيحتاج مراقبة دورية لوظائف الكبد.
• الحمل: تيكفيديرا مش مستحبة للحوامل إلا لو كانت الفوايد تفوق المخاطر، ويفضل استخدام وسائل منع حمل فعالة.
جيلينيا والتيكفيديرا من أوائل الأدوية الفموية اللي غيّرت قواعد علاج التصلب المتعدد، لكن كل واحد فيهم له مميزاته وعيوبه. خلونا نقارن بينهم:
• الفعالية: الدراسات أظهرت إن جيلينيا ممكن يكون أكتر فعالية في تقليل معدل النوبات . لكن الفرق مش كبير جدًا، والتيكفيديرا بيتميز انه بيبطأ تطور الإعاقة في بعض الحالات.
• الآثار الجانبية: الفينجوليمود ليه آثار جانبية أكتر تنوع وممكن تكون أخطر، زي مشاكل القلب و العين . التيكفيديرا آثارها الجانبية أكتر شيوعًا (زي الاحمرار والمشاكل الهضمية) لكنها غالبًا بتكون مؤقتة وأقل خطورة. لكن ضعف المناعة مشكلة في الحالتين .
• الجرعة والاستخدام: جيلينيا جرعة واحدة يومية (0.5 ملجم). ده بيخليه أسهل في الاستخدام من تيكفيديرا اللي لازم تتاخد مرتين يوميًا (240 ملجم) . كمان تيكفيديرا لازم يتاخد مع الطعام وجرعة بداية منخفضة عشان تقلل الآثار الجانبية.
• المراقبة: جيلينيا بيحتاج مراقبة مكثفة في البداية، زي مراقبة القلب لمدة 6 ساعات بعد الجرعة الأولى
• التكلفة والتوفر: الدوائين متوفرين في معظم الأسواق العالمية لكن تكلفتهم مرتفعة . في بعض البلدان زي مصر ممكن تكون تكفيديرا أرخص نسبيًا. لكن لازم نرجع للدكتور والتأمين الصحي عشان التفاصيل.
في النهاية، اختيار الدواء بيعتمد على حالة المريض، تاريخه الصحي، وتفضيلاته . جيلينيا ممكن يكون أفضل للمرضى اللي عندهم نوبات متكررة جدًا ومحتاجين دواء قوي مع جرعة مرة واحدة يوميًا . لكن لازم يكونوا جاهزين للمراقبة المكثفة . تيكفيديرا خيار ممتاز للمرضى اللي عايزين دواء فعال بس مع آثار جانبية أقل خطورة . مع الأخذ في الاعتبار إن الأعراض الهضمية ممكن تكون مزعجة في البداية.
التعليقات مغلقة.
متميز كالعادة
شكرا لذوقك و اتمنى يكون مفيد